L’aura emicranica rappresenta un fenomeno neurologico transitorio e reversibile, che interessa una percentuale significativa dei soggetti affetti da emicrania. Si manifesta attraverso sintomi sensoriali, visivi, motori o linguistici, generalmente precedenti o concomitanti alla fase dolorosa dell’attacco emicranico. Nonostante la sua apparente benignità, l’aura può risultare fonte di notevole disagio e costituire un indicatore di vulnerabilità neurologica. La letteratura neurologica ha da tempo riconosciuto l’importanza di questo fenomeno, che oggi viene analizzato attraverso un approccio multidisciplinare integrato.
Meccanismi fisiopatologici
L’ipotesi patogenetica più accreditata identifica nella cortical spreading depression (CSD) il substrato neurofisiologico primario dell’aura. Tale fenomeno, descritto per la prima volta da Leão (1944), consiste in un’onda di depolarizzazione neuronale seguita da un’inibizione elettrica e da modificazioni del flusso ematico corticale, che si propaga a bassa velocità sulla superficie della corteccia cerebrale.
Durante la CSD si osserva un aumento extracellulare di ioni potassio e glutammato, l’attivazione di astrociti e microglia e la produzione di ossido nitrico (NO) e peptidi vasoattivi, tra cui il calcitonin gene-related peptide (CGRP). Tali modificazioni conducono a una transitoria alterazione dell’omeostasi neuronale e vascolare, configurando una condizione di ipereccitabilità seguita da inibizione funzionale. Le neuroimmagini funzionali (fMRI) hanno documentato la propagazione della CSD nella corteccia occipitale durante episodi di aura visiva (Hadjikhani et al., 2001), offrendo una conferma diretta del suo ruolo.
Un importante contributo è stato fornito dagli studi più recenti di Singh et al. (2024), che hanno evidenziato il coinvolgimento attivo degli astrociti nella propagazione della CSD. Tali cellule gliali, oltre al ruolo di supporto, regolano il microambiente extracellulare attraverso meccanismi di ricaptazione del glutammato e modulazione ionica, incidendo sulla soglia di attivazione e sull’estensione della depolarizzazione.
La fisiopatologia dell’emicrania non può tuttavia essere ridotta al solo fenomeno corticale. Evidenze crescenti indicano il coinvolgimento di strutture sottocorticali, in particolare del tronco encefalico e dell’ipotalamo, nell’innesco e nel mantenimento dell’attacco emicranico. Si ritiene che una disfunzione in queste aree possa alterare il tono dei circuiti trigeminovascolari e della modulazione endogena del dolore (Goadsby et al., 2017). Fluttuazioni del tono neuronale del tronco encefalico possono infatti modificare la soglia di attivazione degli stimoli nocicettivi, favorendo l’innesco dell’aura o della fase dolorosa a partire da stimoli minimi o fisiologici.
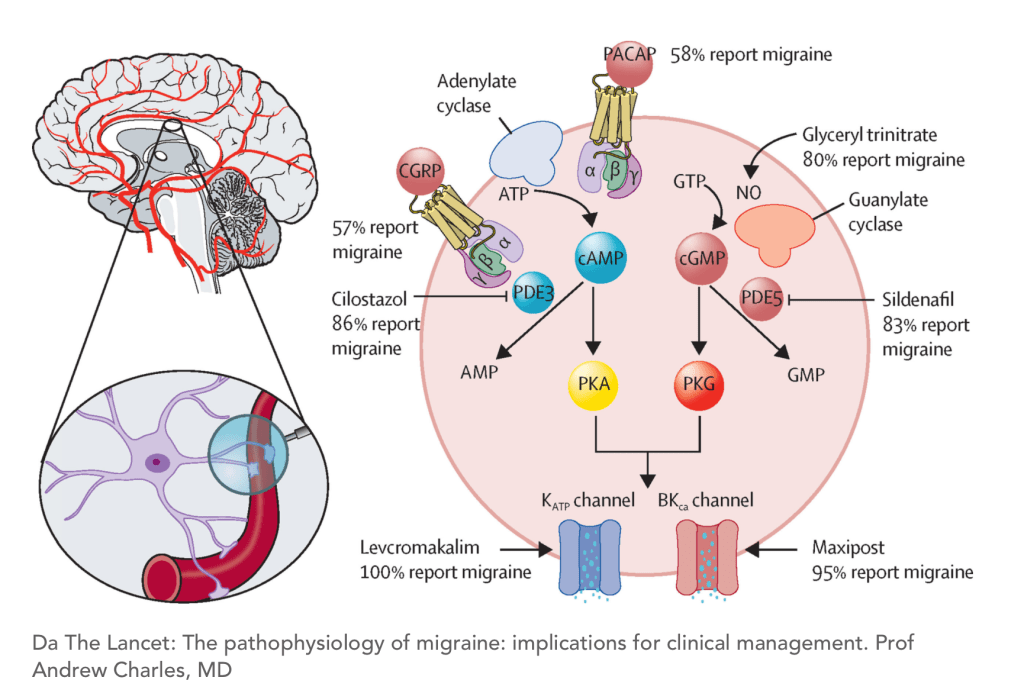
Infine, un ulteriore livello di complessità è fornito dall’identificazione di specifiche vie molecolari intracellulari che regolano la trasduzione del segnale. La stimolazione dei recettori per CGRP, PACAP e NO attiva rispettivamente le vie dell’adenilato e guanilato ciclasi, con produzione di cAMP e cGMP, coinvolgendo le protein chinasi PKA e PKG. Queste vie modulano l’apertura di canali ionici, modificando l’eccitabilità neuronale e la reattività vascolare (Figura 1). Diversi agenti farmacologici che agiscono su queste vie sono stati in grado di evocare attacchi emicranici sperimentalmente, rafforzando l’ipotesi di una vulnerabilità biochimica sottostante.
Manifestazioni cliniche dell’aura
L’aura emicranica si presenta con una varietà di sintomi, la cui natura dipende dalle aree corticali coinvolte. L’aura visiva è la più comune, caratterizzata da scotomi scintillanti, linee a zigzag (fortificazione), alterazioni del campo visivo e visioni luminose o distorte. Le auree sensitive si manifestano con parestesie o ipoestesie che si diffondono gradualmente, spesso partendo dalla mano. Meno frequenti sono le auree afasiche, che compromettono la capacità di espressione o comprensione del linguaggio, e le auree motorie, tipiche dell’emicrania emiplegica, con debolezza muscolare focale. Le forme più rare coinvolgono il tronco encefalico, generando vertigini, disartria, diplopia e, in alcuni casi, compromissione dello stato di coscienza.
La durata tipica di ciascun sintomo auratico è compresa tra 5 e 60 minuti, con risoluzione completa. In casi rari si osservano auree prolungate o persistenti, che sollevano problematiche diagnostiche e richiedono una valutazione neurologica approfondita.

Diagnosi differenziale e classificazione
Secondo i criteri dell’International Classification of Headache Disorders, terza edizione (ICHD-3), l’emicrania con aura si definisce sulla base della progressione graduale, della reversibilità e della tipicità dei sintomi. Tuttavia, nella pratica clinica si pongono frequenti sfide diagnostiche, in particolare nei confronti di attacchi ischemici transitori (TIA), crisi epilettiche focali e disturbi funzionali. La distinzione si basa sulla durata dei sintomi, sulla loro progressione, sull’eventuale presenza di dolore associato e sul contesto clinico. Una revisione sistematica (Joppeková et al., 2025) ha suggerito l’ampliamento dei criteri attuali per includere forme atipiche o isolate.
Genetica e predisposizione
L’emicrania con aura presenta una componente ereditaria. Nelle forme monogeniche, come l’emicrania emiplegica familiare, sono implicati geni che codificano per canali ionici (CACNA1A, SCN1A, ATP1A2). Nelle forme comuni si osserva una predisposizione poligenica, con loci associati all’eccitabilità neuronale, alla trasmissione sinaptica e alla regolazione vascolare. Studi recenti hanno ipotizzato il coinvolgimento di meccanismi epigenetici e di uno stato pro-infiammatorio subclinico, che potrebbero abbassare la soglia per la CSD e facilitare l’espressione clinica dell’aura.
Trattamento
Non esistono terapie specifiche per l’aura in sé, ma interventi mirati all’intero spettro dell’emicrania. Il trattamento acuto comprende l’impiego di FANS e triptani, efficaci nella fase dolorosa ma non sulla sintomatologia auratica. Nuove classi di farmaci, quali gepanti (antagonisti CGRP) e ditani (agonisti 5-HT1F), stanno emergendo come opzioni promettenti, sebbene le evidenze sulla loro efficacia sull’aura siano ancora limitate.
Per la profilassi si impiegano betabloccanti, calcio-antagonisti, antiepilettici (es. topiramato), antidepressivi triciclici e, più recentemente, anticorpi monoclonali anti-CGRP. Questi ultimi hanno dimostrato efficacia nella riduzione della frequenza degli attacchi, ma il loro impatto sull’incidenza dell’aura richiede ulteriori approfondimenti. Approcci non farmacologici – come biofeedback, tecniche di rilassamento, neurostimolazione vagale e supporto psicologico – possono integrare efficacemente la gestione clinica.
Prospettive
L’aura emicranica costituisce un modello paradigmatico per lo studio della disfunzione cerebrale transitoria. Essa permette di esplorare i limiti della fisiologia corticale, offrendo una finestra sulle modalità con cui il cervello genera percezioni anomale ma strutturate. L’interazione tra eventi corticali, dinamiche sottocorticali e segnalazioni molecolari disegna un quadro complesso in cui la vulnerabilità individuale si traduce in una risposta clinica specifica.
Le future ricerche dovranno approfondire le interazioni glia-neurone, il ruolo dell’infiammazione cerebrale, la genetica funzionale e i meccanismi di cronicizzazione. L’obiettivo è quello di sviluppare interventi terapeutici personalizzati, capaci di agire precocemente sulla soglia di attivazione della crisi emicranica, prevenendo la disabilità e migliorando la qualità di vita dei pazienti.
Bibliografia
Coerver, K. A., & Subramanian, P. S. (2020). Visual hallucinations in psychiatric, neurologic, and ophthalmologic disease. Current Opinion in Ophthalmology, 31(6), 475–482. https://doi.org/10.1097/ICU.0000000000000700
Coppola, G., & Di Lorenzo, C. (2017). La fisiopatologia dell’aura emicranica: dalla ricerca alla clinica. Giornale delle Cefalee, 13(2), 1–2.
Di Piero, V., & Gilliéron, E. R. (2022). Cefalea: dal dolore alla sofferenza dell’anima. Roma: Sapienza Università Editrice.
Hadjikhani, N., Sanchez Del Rio, M., Wu, O., Schwartz, D., Bakker, D., Fischl, B., Kwong, K. K., Cutrer, F. M., Rosen, B. R., Tootell, R. B. H., Sorensen, A. G., & Moskowitz, M. A. (2001). Mechanisms of migraine aura revealed by functional MRI in human visual cortex. Proceedings of the National Academy of Sciences, 98(8), 4687–4692. https://doi.org/10.1073/pnas.071582498
Joppeková, Ľ., Hlušíková, M., Kaňuchová, M., Hlušík, D., Gdovinová, Z., & Szilasiová, J. (2025). What does a migraine aura look like? A systematic review. The Journal of Headache and Pain, 26(149). https://doi.org/10.1186/s10194-025-02080-6
Leão, A. A. P. (1944). Spreading depression of activity in the cerebral cortex. Journal of Neurophysiology, 7(6), 359–390. https://doi.org/10.1152/jn.1944.7.6.359
Sacks, O. (2010). Emicrania. Milano: Adelphi. (Titolo originale: Migraine, 1970)
Singh, B., Han, J. H., Wang, Y., Lee, H., Kim, J., Park, J., Kim, Y., & Lee, M. (2024). Astrocytes orchestrate cortical spreading depolarization by regulating extracellular potassium and glutamate. PLOS Biology, 22(6), e3003168. https://doi.org/10.1371/journal.pbio.3003168
Lascia un commento